Группа российских исследователей показала, что инвазия опухоли — это не просто разрушение тканей, а сложный адаптивный процесс коллективной миграции опухолевых клеток. Во время него метастазы становятся новыми центрами инвазии и инициируют дальнейшее распространение опухоли. Исследование поддержано грантом Российского научного фонда № 24-25-0047 и опубликовано в международном рецензируемом журнале Cancers.
Несмотря на развитие методов диагностики и лечения, рак остается одной из ведущих причин смертности во всем мире. Однако процесс распространения рака в организме человека во время инвазии и метастазирования — основных причин смерти при развитии онкологических заболеваний — до сих пор изучен недостаточно подробно. Кроме того, рак обладает феноменальной способностью адаптироваться к неблагоприятным условиям, например, к применению противоопухолевой лекарственной терапии. Поэтому все большее значение приобретают фундаментальные исследования механизмов развития онкологических заболеваний.
Российские ученые впервые в мире детально изучили процессы инвазии и метастазирования методом рентгеновской компьютерной микротомографии. Использование этого метода, который дает возможность изучать ткани с помощью рентгеновского излучения без их разрушения, позволило исследователям впервые визуализировать процессы инвазии и метастазирования в трехмерном пространстве с микроскопическим разрешением. Такой подход значительно расширяет возможности анализа пространственной организации опухоли. Опухолевая ткань хуже задерживает рентгеновское излучение и, соответственно, обладает меньшей рентгеновской плотностью, чем ткань здоровых, неповрежденных органов, что показано на шкале рентгеновской плотности (рисунок 1, слева), поэтому микротомография позволяет точно определить их расположение относительно друг друга в трехмерном пространстве. На рисунке 1 показан процесс распространения опухоли через брюшину в анатомической области между селезенкой, желудком и поджелудочной железой. На поверхности селезенки виден опухолевый очаг, который сформировался в результате перемещения клеток через брюшину. Этот очаг не только прорастает в ткань селезенки (показано стрелкой, слева), но и стелется по брюшине, покрывающей желудок, без ее разрушения, достигая поджелудочной железы и проникая в ее ткань (показано стрелкой, справа). Опухоль использует брюшину как удобную среду для распространения (подобно дорогам или рельсам), минимизируя разрушение тканей и адаптируясь к ее структуре.
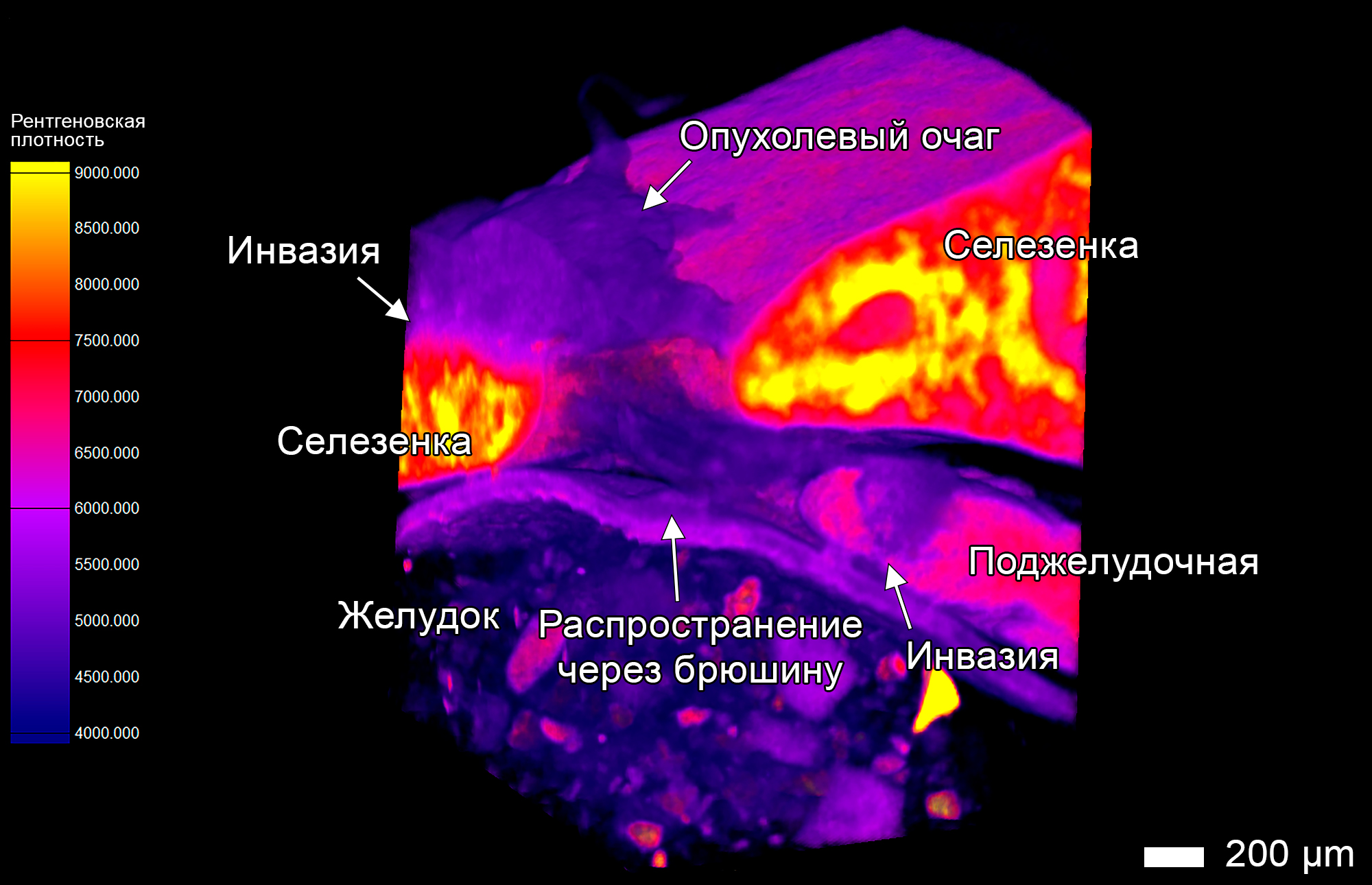
Рисунок 1. Распространение опухоли через брюшину в поджелудочную железу
«Гистологическое исследование, которое широко применяется врачами-патологоанатомами для диагностики онкологических заболеваний, позволяет получить только плоские, двумерные срезы опухоли и окружающих здоровых тканей. Для точной диагностики заболеваний гистологическое исследование является золотым стандартом диагностики, однако на плоских срезах невозможно проследить, как именно опухоль распространяется в живой ткани. Поэтому мы значительно увеличили точность визуализации опухолевой прогрессии, комбинируя микротомографию и гистологию. Кроме того, результаты исследования также раскрывают перспективы для клинической онкологии. Рентгеновская микротомография может стать частью комплексного исследования органов, удаленных после операции, может повысить точность стадирования онкологических заболеваний, поскольку мы можем детально визуализировать прорастание опухоли в сосуды, нервы, метастатическое поражение лимфатических узлов в трехмерном пространстве. Также разрабатываются методы исследования опухолевых тканей, заключенных в парафиновые блоки, а также нативного материала, полученного после секторальной резекции молочной железы, резекции легкого, биоптатов костной ткани. Разрабатываются новые протоколы подготовки проб, которые в будущем могут значительно ускорить исследование операционного и биопсийного материала, а также стать инструментом для мониторинга лечебного патоморфоза опухоли», — отмечает Сергей Ткачев, руководитель исследования, младший научный сотрудник Института регенеративной медицины Сеченовского Университета.
Ученые смоделировали развитие плоскоклеточного рака пищевода: полученные от пациента фрагменты опухоли были пересажены иммунодефицитным мышам, что позволило воспроизвести процесс инвазии и метастазирования. С помощью рентгеновской микротомографии и гистологического исследования сопоставимых зон интереса исследователи смогли детально изучить, как раковые клетки проникают в окружающие ткани, формируют метастазы и взаимодействуют с микроокружением.
Исследование показало, что адаптивная фенотипическая пластичность может приводить к изменению форм, свойств и поведения клеток опухоли в зависимости от тканевого микроокружения, что приводит к выживанию и инвазии клеток даже в условиях недостатка кислорода или агрессивного лечения. Адаптивная фенотипическая пластичность также обеспечивает сетевое, циклическое распространение рака. Метастазы, образовавшиеся на расстоянии от первичной опухоли, могут стать новыми центрами роста и инвазии, поддерживая процесс распространения опухоли. Такой механизм превращает рак в самоподдерживающуюся сеть, что объясняет сложности при лечении метастатических опухолей. Данное исследование предоставляет значительные данные в поддержку концепции циклического распространения рака и реципрокного взаимодействия между опухолью и окружающими тканями, выдвинутую исследователем-онкологом Питером Фридлем еще в 2011 году, согласно которой метастазы могут становиться активными центрами инвазии, продолжая процесс распространения опухоли.
Полученные данные открывают новые возможности для разработки терапевтических стратегий, направленных на разрушение циклического процесса инвазии. Таргетные препараты, воздействующие на лидерные клетки или механизмы адаптивной пластичности, могут стать ключевыми в борьбе с метастатическими опухолями.
По мере вторжения опухолевые клетки не просто разрушают ткани, но и адаптируются к различным условиям, используя доступные структуры для продвижения. Например, в плотной ткани селезенки они формируют пальцевидные выросты, вторгаясь в ткань органа, а на поверхности органов — распространяются тонкими слоями, скользя по тканям, не разрушая их. На рисунке 2 показано распространение опухоли из первичного очага, находящегося на поверхности желудка. Для своего распространения опухоль использует перемещение по брюшине, не разрушая ее, чтобы сформировать новые метастатические очаги в другой области желудка и на поверхности селезенки.
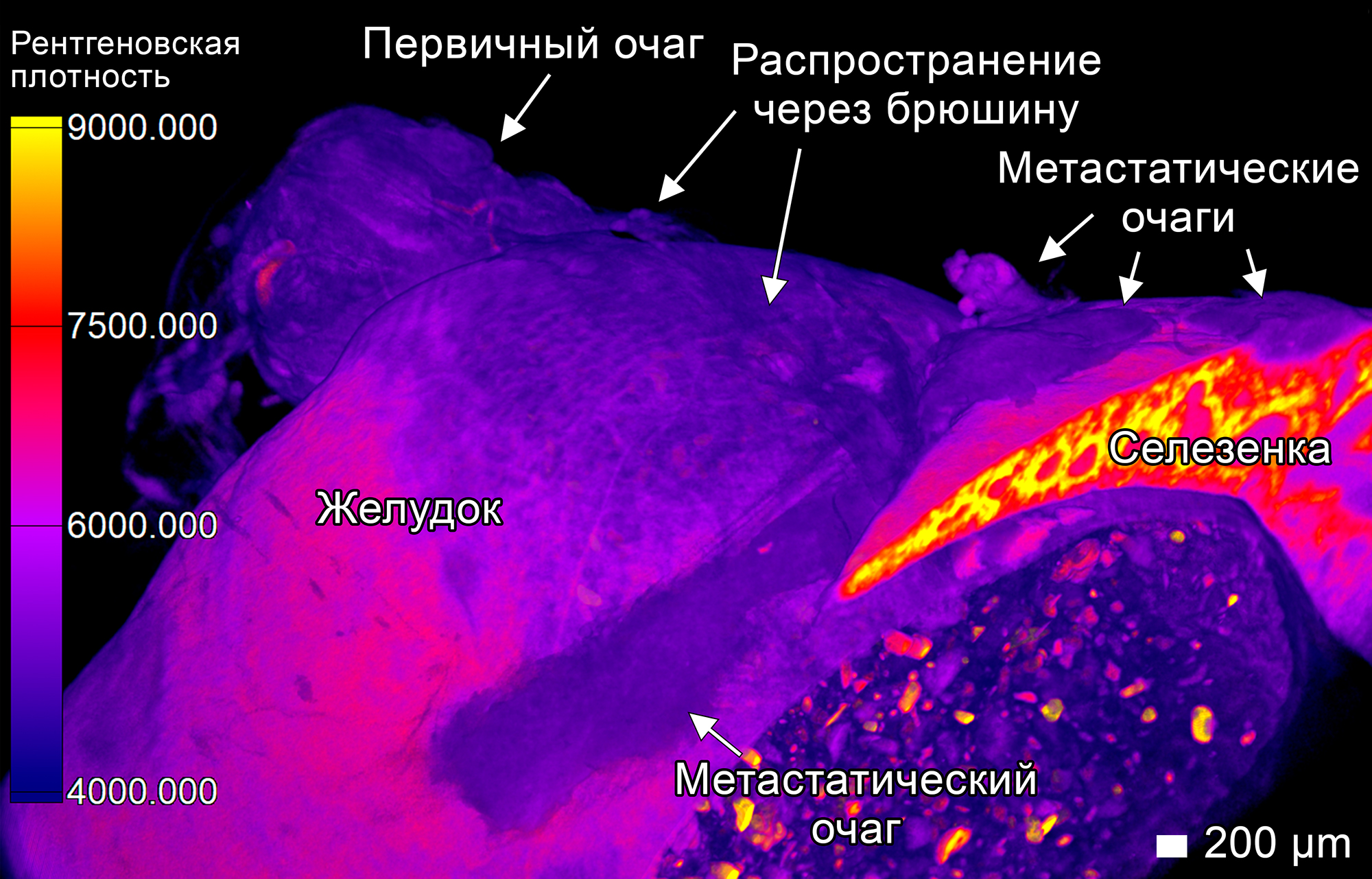
Рисунок 2. Распространение опухоли по брюшине, покрывающей желудок, с формированием новых метастатических очагов на поверхности желудка и селезенки
Одним из ключевых открытий стало обнаружение различных паттернов инвазии, включая формирование пальцевидных выростов (finger-like projections), которые ранее были недоступны для изучения в двухмерных гистологических срезах. Этот процесс — коллективная миграция — является ключевой стратегией рака для выживания и дальнейшего распространения. На рисунке 3 показано, как из опухолевой массы формируется опухолевый тяж (stand) с лидерными клетками, который внедряется в слои стенки желудка и разделяет ее мышечную и слизистую оболочку. Такое поведение опухолевых клеток функционально напоминает коллективную миграцию простейших организмов, таких как социальные амебы (известные как грибы-слизевики) Dictyostelium и Fonticula alba. Их движение скоординировано: лидерные клетки прокладывают путь, а клетки-последователи поддерживают процесс миграции. Эти данные поддерживают гипотезу о том, что в ходе прогрессии опухоли запускаются эволюционно древние программы клеточной активности, схожих с механизмами поведения одноклеточных организмов, что обеспечивает выживание и распространение клеток.
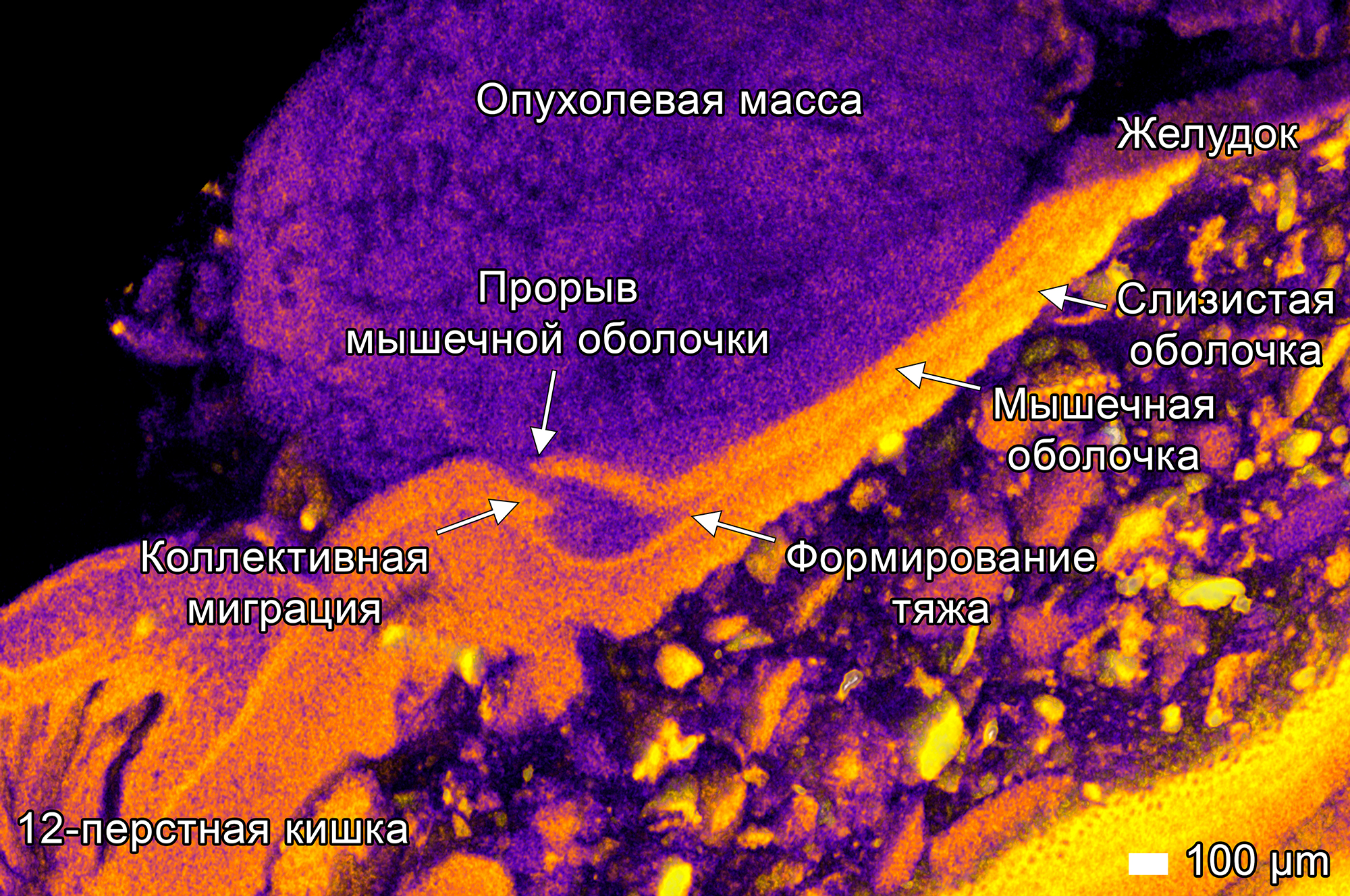
Рисунок 3. Коллективная миграция опухолевых клеток с внедрением в слои стенки желудка
Феномен опухолевого почкования (tumor budding), который выглядит как появление при гистологическом исследовании изолированных скоплений раковых клеток, отделяющихся от основной массы опухоли (рисунок 4, справа), может быть артефактом подготовки гистологических препаратов. На микротомографическом изображении показано, что опухолевые почки связаны с основной массой опухоли, а при трехмерной визуализации являются пальцевидными выростами (рисунок 4, слева). Полученные результаты ставят под вопрос интерпретацию наличия и количества опухолевых почек в эпителиальных опухолях при гистологическом исследовании. Однако, несмотря на то, что эти структуры могут быть артефактами подготовки образцов, в настоящий момент наличие опухолевых почек остается одним из важных прогностических факторов как в плоскоклеточном раке пищевода, так и в раке толстой кишки. Дальнейшие исследования с помощью рентгеновской микротомографии могут уточнить происхождение опухолевых почек, их природу и роль в опухолевом процессе.
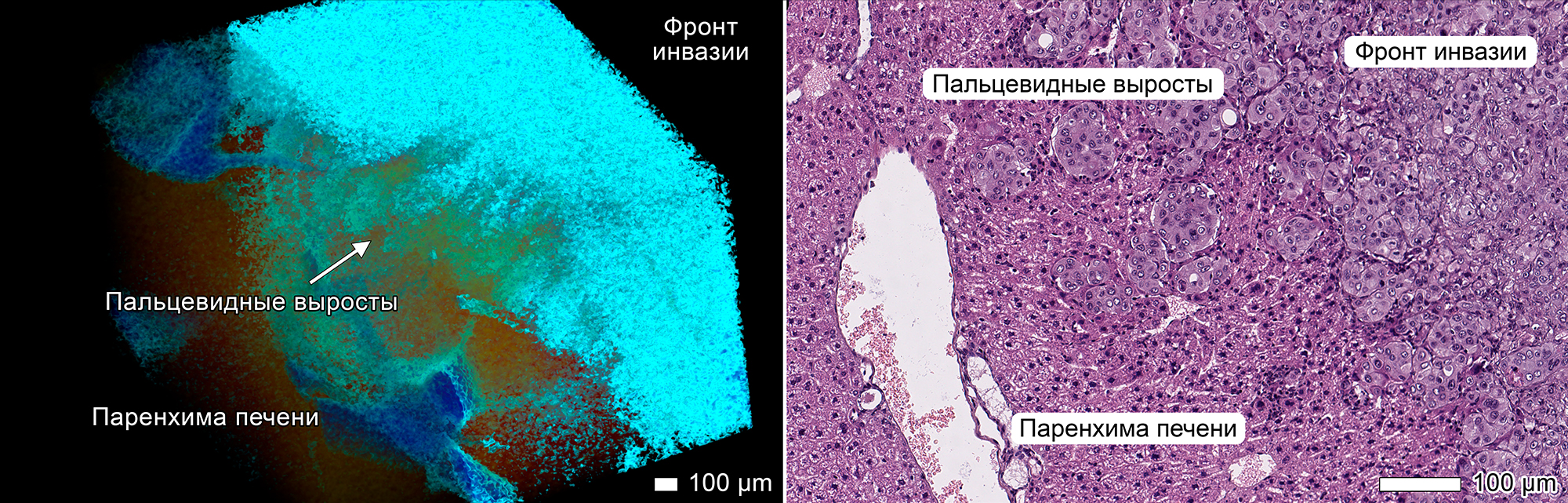
Рисунок 4. Пальцевидные выросты опухолевой ткани в печени, трехмерное микротомографическое изображение и двухмерный гистологический срез.
Перитонеальный канцероматоз — не случайный процесс распространения опухолевых клеток, а их организованное перемещение по брюшине. Опухоль использует брюшину как путь для своего распространения, адаптируясь к ее структуре и минимизируя ее разрушение (рисунок 5).
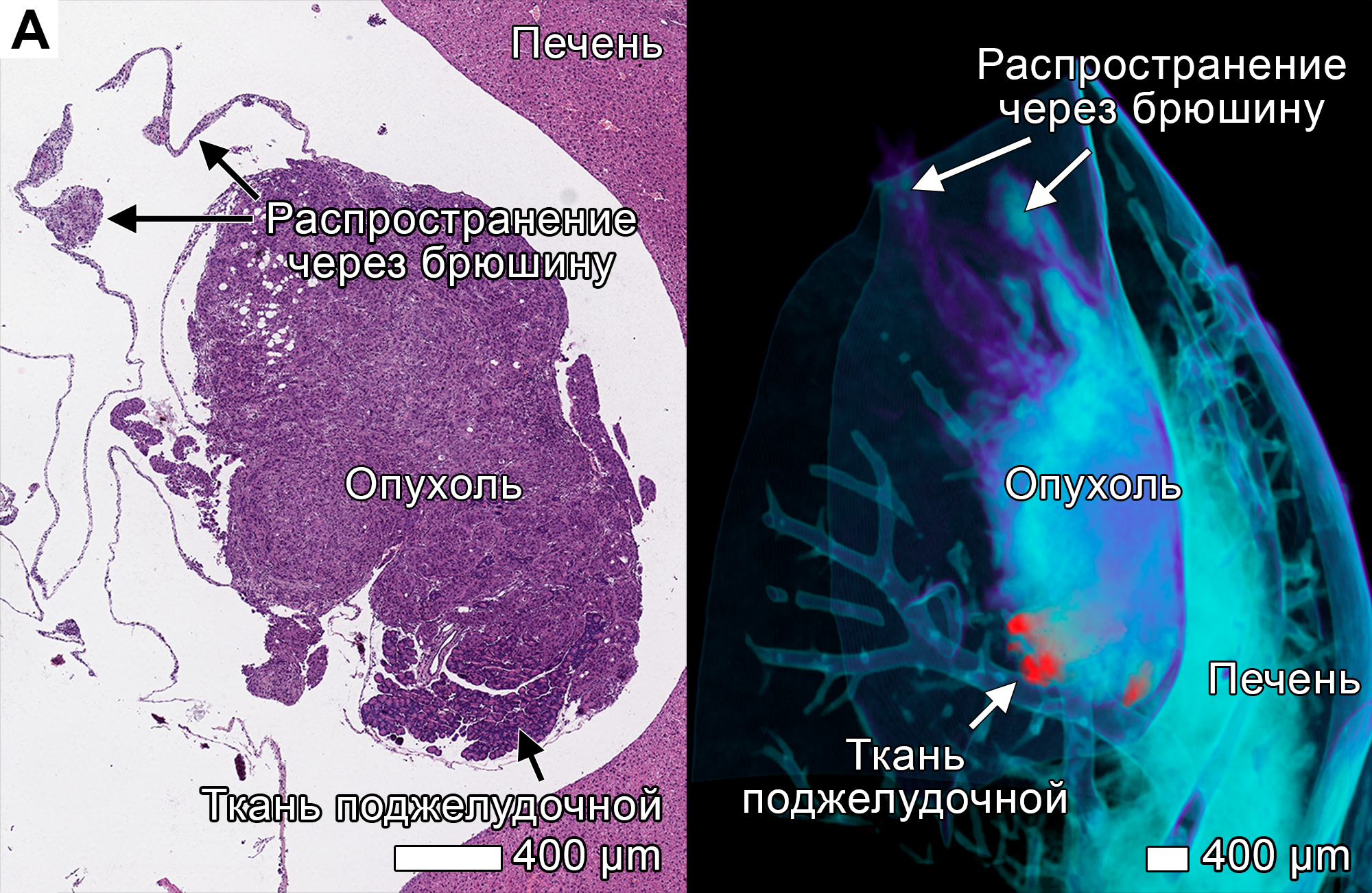
Рисунок 5. Распространение опухоли по брюшине
Таким образом, результаты исследования указывают, что общепринятые подходы к лечению метастатических форм рака стоит переосмыслить. Стратегии, направленные на прерывание циклического процесса инвазии и метастазирования, могут стать ключом к разработке более эффективной терапии.
Исходные данные исследования, полученные с помощью рентгеновской микротомографии, позволяющие воспроизвести находки при эксперименте, доступны по ссылке. Над проектом работала мультидисциплинарная команда ученых со всей России: из Сеченовского Университета (Сергей Ткачев, Петр Тимашев), Медицинского института Пензенского государственного университета (Владимир Бросалов), Национального медицинского исследовательского центра онкологии в Ростове-на-Дону (Олег Кит, Алексей Максимов, Анна Гончарова), Донского государственного технического университета (Евгений Садырин), Института молекулярной биологии имени В.А. Энгельгардта (Александра Далина), Федерального научно-клинического центра ФМБА (Елена Попова), Сибирского государственного медицинского университета (Антон Осипенко), Московского научно-клинического центра имени А.С. Логинова (Николай Карнаухов, Марк Волошин).
«Эта работа посвящается нашему дорогому другу, коллеге, ученому, преподавателю и врачу-патологоанатому Владимиру Бросалову, который внес неоценимый вклад в это исследование, начиная от его концептуализации и заканчивая анализом микротомографических и гистологических изображений и созданием текста рукописи. Владимир покинул нас слишком рано, но мы продолжим развивать его идеи в дальнейших исследованиях. Эта работа — свидетельство того огромного пути, который мы начали вместе, и той преданности делу, на которую он вдохновил нас», — заключают авторы исследования.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.