Ученые из США и Бельгии смогли синтезировать метанол из метана при комнатной температуре, используя в качестве катализатора цеолиты железа. Изучив строение кристаллов цеолитов железа, ученые добились повторной активации 40% активных сайтов катализатора. Открытие может стать важным шагом на пути к созданию топливных элементов нового поколения. Статья опубликована в журнале Science.
Метанол — простейший спирт и основной компонент природного газа, использующийся для изготовления краски и пластмассы, а также в качестве добавки к бензину. Благодаря высокому содержанию водорода он перспективен для применения в топливных элементах нового поколения, не загрязняющих окружающую среду. Если бы природный газ можно было экономично преобразовать в метанол, полученное жидкое топливо было бы намного легче хранить и транспортировать. Это также значительно сократило бы выбросы метана в атмосферу. Ученые из Стэнфордского и Левенского университетов усовершенствовали один из способов получения метанола.
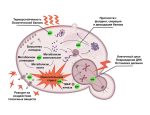
Обычно в этом процессе используются кристаллы — цеолиты железа, которые катализируют реакцию при комнатной температуре. В порах кристалла метанол образуется при комнатной температуре без дополнительных затрат тепла или энергии. Тогда как в промышленном производстве метанола из метана требуется температура около 1000 °C и чрезвычайно высокое давление. Однако вывести синтез с помощью цеолитов на промышленный уровень непросто, так как этот катализатор быстро дезактивируется.
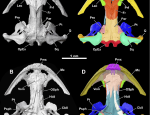
Изучив структуру разных железных цеолитов, авторы обнаружили, что их реакционная способность резко меняется в зависимости от размера пор в кристаллической структуре. Если поры слишком велики, активный центр деактивируется после единственного цикла реакции и больше не активируется. Однако, когда поры меньше, они могут координировать реакцию и регенерировать. Подобрав нужный размер пор, ученые смогли повторно активировать 40% активных сайтов.
Кроме того, ученые использовали в качестве источника кислорода воздух, а не закись азота, которая используется обычно. Такой мощный окислитель, как кислород, трудно контролировать в химических реакциях. Поэтому открытие устраняет еще одно препятствие.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.