Ученые из Брукхейвенской национальной лаборатории (США) разработали модель, которая показывает, как белок вируса SARS-CoV-2 захватывает белок клеточного соединения, поддерживающего слизистую оболочку легких. Разработка поможет объяснить, каким образом вирус вызывает обширное повреждение легких и заражает другие органы. Полученные результаты могут ускорить поиск лекарств, предотвращающих наиболее тяжелые последствия заболевания. Работа опубликована в журнале Nature Communications.
«Получив подробности взаимодействия белков на атомарном уровне, мы можем объяснить, почему происходит повреждение, и искать ингибиторы, которые могут блокировать эти взаимодействия, — сказал ведущий автор исследования Цюнь Лю, структурный биолог из Брукхейвенской лаборатории. — Если мы сможем найти ингибиторы, то вирус не причинит такого большого вреда. Это может дать людям с ослабленным здоровьем гораздо больше шансов успешно побороть вирус».
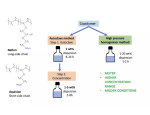
Ученые разработали молекулярную модель, используя один из новых криоэлектронных микроскопов в Лаборатории биомолекулярной структуры (LBMS).
«LBMS предлагает дополнительные методы визуализации, которые играют важную роль в расшифровке белков, участвующих в COVID-19. Это первая статья, опубликованная на основе результатов работы нового объекта», — рассказал Шон Мак-Суини, директор LBMS и соавтор статьи.
Криоэлектронная микроскопия полезна при изучении мембранных белков и белковых комплексов. С помощью этой методики ученые создали 3D-карту, благодаря которой смогли зафиксировать динамические взаимодействия между белками.
Белок оболочки SARS-CoV-2 (E), который находится на внешней мембране вируса, помогает собирать новые вирусные частицы внутри инфицированных клеток. Исследования, опубликованные в начале пандемии COVID-19, показали, что он также играет решающую роль в захвате белков для дальнейшего распространения вируса. Ученые предполагают, что это происходит при нарушении соединений между клетками легких. В таком случае иммунные клетки пытаются исправить повреждение, высвобождая белки, называемые цитокинами. Этот иммунный ответ может усугубить ситуацию, вызвав массивное воспаление, вызывающее так называемый цитокиновый шторм и последующий острый респираторный дистресс-синдром.
Более того, повреждение межклеточных связей может облегчить вирусам выход из легких и попадание через кровоток в другие органы, включая печень, почки и кровеносные сосуды.
«В этом случае большинство повреждений произойдет у пациентов с большим количеством вирусов и большим количеством белков E, — добавил Цюнь Лю. — Из-за этого образуется порочный круг — чем больше вирусов, тем больше белков Е и больше поврежденных клеточных соединений, которые провоцируют дальнейшее распространение вируса. Кроме того, любые повреждения, например рубцы на легочных тканях, затруднят восстановление пациентов после перенесенного COVID-19. Поэтому мы хотели понять, как прервать цепочку и уменьшить или остановить развитие серьезных осложнений».
Разработанная модель содержала достаточно информации об уникальных характеристиках отдельных аминокислот, входящих в состав двух белков, благодаря чему ученые смогли вписать известные структуры этих аминокислот в карту и объяснить, каким образом происходит повреждение клеток.
«Эта структура обеспечивает основу для поиска лекарств, которые могут блокировать распространение повреждений», — сказал соавтор статьи Джон Шенклин, председатель биологического отдела Брукхейвенской лаборатории.
Понимание динамики этого белкового взаимодействия также поможет ученым проследить, как развиваются вирусы, подобные SARS-CoV-2.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.