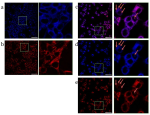
Британские ученые показали, что короноподобные структуры, образованные макрофагами вокруг опухолей молочной железы у пациентов с избыточной массой тела, могут затруднять терапию. Исследователи также описали потенциальный молекулярный биомаркер, по наличию которого можно прогнозировать ответ на лечение. Результаты исследования позволят подбирать терапию индивидуально для каждого пациента. Статья опубликована в журнале Scientific Reports.
Жировая ткань является неотъемлемым компонентом здоровой молочной железы. Однако высокий индекс массы тела (ИМТ) связан с повышенным риском развития рака груди и худшими показателями выживаемости. У пациентов с высоким ИМТ увеличение жировых отложений может приводить к скоплению воспалительных иммунных клеток макрофагов в ткани груди. Они же могут образовывать так называемые «короноподобные структуры», окружая жировые клетки и создавая воспаление, которое может привести к возникновению и росту опухолей.
Ученые из Саутгемптонского университета исследовали образцы тканей пациентов с раком молочной железы положительным по рецептору человеческого эпидермального фактора роста 2 типа (HER2+). Они искали связь высокого ИМТ и количества короноподобных структур, а также оценивали их влияние на реакцию пациентов на терапию препаратом трастузумабом. Оказалось, что пациенты с избыточным весом или ожирением имели значительно больше короноподобных структур. Это было связано также с быстрым метастазированием и плохой реакцией на терапию.
Затем ученые идентифицировали потенциальный молекулярный биомаркер CD32B на поверхности макрофагов короноподобных структур. Когда он присутствовал, у пациентов с избыточной массой тела и ожирением ответ на терапию трастузумабом был хуже. Результаты работы потенциально могут быть использованы для разработки персонализированного лечения пациентов с HER2+ раком молочной железы.
«Например, врачи должны знать, что пациенты с высоким ИМТ и маркером CD32B, вероятно, будут плохо реагировать на терапию трастузумабом. Поэтому им может помочь более интенсивная анти-HER2-терапия на ранних этапах лечения, — говорит соавтор исследования Стивен Бирс. — С другой стороны, это исследование показывает, насколько эффективно лечение трастузумабом у пациентов, у которых нет маркера. Эти пациенты могут получить пользу от более низкой дозы анти-HER2-терапии, которая сведет к минимуму побочные эффекты. Для подтверждения этих первоначальных результатов потребуются дальнейшие исследования с большим количеством пациентов».
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.