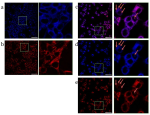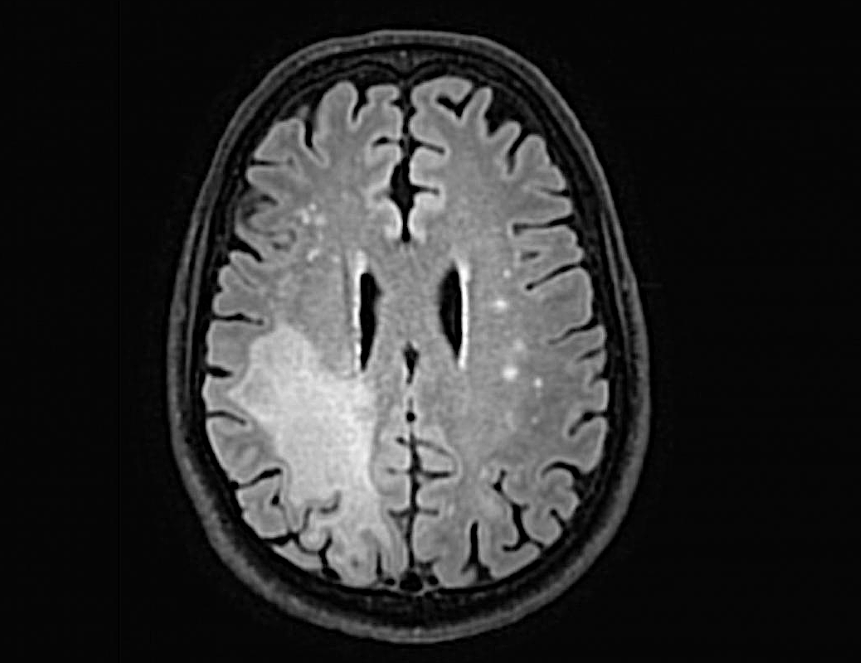
Ученые смоделировали лейкоэнцефалопатию с исчезающим белым веществом (Vanishing White Matter Disease, VWMD), которая вызывает серьезные проблемы с нервной системой у детей. Ученые обнаружили, что клетки, несущие ген, вызывающий это заболевание, имеют мутации в белке, который обычно помогает клеткам справляться с различными видами стрессовых воздействий. Однако эти клетки с мутацией адаптируются и функционируют нормально до момента стресса, после чего они быстро разрушаются. Это открытие показало адаптивную реакцию клеток на стресс, которую ученые назвали «разделенной интегрированной реакцией на стресс» (s-ISR). Результаты исследования могут помочь в разработке новых методов лечения рака и заболеваний нервной системы, таких как рассеянный склероз и боковой амиотрофический склероз. Работа опубликована в журнале Nature.
Когда клетки нашего организма сталкиваются со стрессом (токсины, мутации, окисление или недостаток питательных веществ), их нормальное функционирование нарушается, ставится «на паузу». Это позволяет им сосредоточиться на сохранении энергии, замене поврежденных компонентов и укреплении защиты. Если стресс не слишком сильный, клетки могут вернуться к нормальной работе. В противном случае они могут самоуничтожиться. Обычно считалось, что при клеточном стрессе «включается сигнал тревоги», при котором белки начинают замедлять или останавливать нормальную работу клетки.
Обычно при стрессе начинается фосфорилирование белка eIF2α, который работает фактором инициации трансляции. Но теперь ученые нашли новый механизм реакции клеток на стресс. Они назвали эту адаптивную реакцию «разделенной интегрированной реакцией на стресс» (s-ISR). В отличие от обычной реакции на стресс, s-ISR запускается снижением активности другого белка, eIF2B. Это происходит без фосфорилирования eIF2α и приводит к другим изменениям в клетке. Фосфорилирование — это процесс, при котором к молекуле добавляется остаток фосфорной кислоты, что меняет ее активность и часто используется для регулирования функций белков. Исследователи показали, что реакция клеток на стресс гораздо более сложная и гибкая, чем считалось ранее.
«Это исследование представляет собой новый взгляд на клеточный стресс. ISR — это не универсальная система, как мы думали раньше. Напротив, она может меняться и подстраиваться в зависимости от типа, силы и продолжительности стресса, который испытывает клетка», — отметила Мария Хатзоглу из Университета Кейс-Вестерн-Резерв, США.
Исследователи изучали лейкоэнцефалопатию с исчезающим белым веществом (Vanishing White Matter Disease, VWMD) у детей. Болезнь приводит к серьезным проблемам, таким как трудности с движением, судороги и спад умственных способностей. Они обнаружили, что клетки с генетическими мутациями, вызывающими это заболевание, имеют изменения в белке eIF2B, который отвечает за регулирование синтеза белков в клетке. Однако мозговые клетки адаптируются к этим нарушениям и в основном работают нормально, но они очень уязвимы и самоуничтожаются даже при незначительном стрессе.
Когда исследователи снижали активность eIF2B в клетках мышей, это не вызывало те же реакции стресса, что и при обычном стрессе, когда активируется белок eIF2α-p. В нормальных условиях снижение активности eIF2B не приводит к образованию стрессовых гранул, которые обычно появляются при стрессе. Однако это снижение активности все равно влияет на синтез белков, особенно на те, которые важны для выживания клетки в стрессовых условиях. Например, снижение активности eIF2B может привести к увеличению производства белка ATF4, который помогает клетке адаптироваться к стрессу. При этом оно не вызывает активацию других белков, которые обычно включаются при стрессе, таких как GADD34, BiP и CHOP. Это показывает, что снижение активности eIF2B в отсутствие стресса включает другие механизмы, отличные от тех, которые срабатывают при обычном стрессе.
Такая адаптация клеток объясняет, почему пациенты с этим заболеванием испытывают значительный спад умственных и двигательных способностей после даже незначительных стрессов, таких как лихорадка или легкая черепно-мозговая травма. Аналогичные механизмы могут работать и в других заболеваниях нервной системы, таких как рассеянный склероз и боковой амиотрофический склероз (ALS).
Понимание этой адаптации может помочь в разработке новых методов лечения рака и заболеваний нервной системы. Ученые планируют исследовать устойчивые к химиотерапии клетки рака молочной железы, чтобы лучше понять, как эти клетки адаптируются к стрессу, и найти новые методы лечения.
Автор: Оксана Гриценко.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.