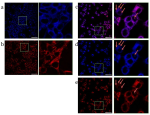
Эпитопы — части макромолекулы антигена, которые помогают клеткам иммунной системы отличать здоровые ткани от чужеродных и больных. Теперь ученые, проанализировав 6 тысяч случаев рака молочной железы (РМЖ), выявили зависимость течения заболевания от набора эпитопов. У агрессивных опухолей количество эпитопов на поверхности клеток больше, чем у новообразований, не склонных к метастазам. Исследование опубликовано в журнале Science.
Многоклеточный организм может функционировать только под защитой иммунной системы. Ее задача — отыскивать, распознавать и уничтожать как внешних агрессоров (бактерии, грибки, вирусы), так и внутренних — старые, больные и «перерождающиеся» клетки. В ее основе лежит взаимодействие антигена (своеобразного «паспорта» на поверхности клеток) с антителом («пограничником» иммунной системы). Комплекс «антиген — антитело» может связывать токсины или микроорганизмы, но главное — он передает сигналы на дальнейшие звенья иммунной реакции, в результате которой организм разными путями уничтожает врага, несущего антиген. Иммунные клетки отличают здоровые клетки от аномальных благодаря главному комплексу гистосовместимости (МНС). У клеток с измененным метаболизмом, стареющих, пораженных вирусом или измененных опухолевым процессом МНС будут иметь видоизмененные эпитопы, так как проблемы в синтезе белка неизменно будут сказываться на их качестве — они отличаются по пространственному строению от нормальных. Именно эти небольшие пептиды ответственны за то, будут ли клетки, несущие мутацию, распознаваться и уничтожаться Т-лимфоцитами и натуральными киллерами или ускользнут от иммунных защитников и создадут новообразование.
Некоторые гены изначально существенно повышают риск развития рака, например BRCA1, BRCA2 и TP53. Они передаются по наследству и нарушают ход деления клетки и процесс исправления ошибок в ДНК. Однако существуют десятки или сотни онкогенов, которые определяют «предрасположенность» к новообразованиям и степень их агрессивности не так явно.
Исследователи занялись поиском генетических маркеров, способных помочь прогнозировать возникновение и течение рака молочной железы. С помощью машинного обучения ученые собирали данные о мутациях, возникающих в клетках, пораженных раком молочной железы. На основе 5870 случаев исследователям удалось выявить одиннадцать подтипов рака молочной железы с различными прогнозами и риском рецидива. Они обнаружили, что в четырех из одиннадцати групп вероятность рецидива значительно выше даже через 10 или 20 лет после диагностики и лечения. Одним из генетических маркеров оказались мутации в генах регуляторных путей, которые тонко настраивают развитие клетки и обеспечивают «уверенность» в выбранном пути. Результат работы этих генов — правильные эпитопы на поверхности МНС. У раковых клеток за счет ошибок этих генов нет контроля синтеза белка, в том числе МНС. Мутации выглядят как множество копий нормального гена в ДНК — результат геномного повторения, называемого амплификацией. Этот процесс в отношении конкретных онкогенов запускает различные пути развития рака и использовался для отличия одного подтипа рака молочной железы от другого.
«На ранней, доинвазивной стадии высокая нагрузка эпитопов на поверхности клеток защищает от рака, привлекая больше Т-лимфоцитов. Картина меняется по мере прогрессирования опухоли: как только им приходится бороться с иммунной системой, новообразования с высоким содержанием эпитопов становятся более агрессивными и склонными к метастазированию», — рассказала Кэтрин Хулахан из Стэнфордского университета.
Большинство опухолевых клеток, постоянно появляющихся при воздействии разных токсических веществ, ошибок деления и других случайных событий, устраняются иммунными клетками и остаются незамеченными. Однако иммунная система не всегда побеждает. Те клетки, которым на ранних этапах удалось скрыться, развивают способы уклонения от иммунного распознавания и разрушения. Результаты исследования могут указать оптимальные сроки терапевтического вмешательства, а также то, как сделать опухоль более чувствительной к терапии. Новые генетические маркеры и основанное на них разделение РМЖ на 11 подтипов может помочь в уточнении прогноза, а также в правильном подборе тактики лечения для пациентов с этим заболеванием.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.